鄭州源創(chuàng)基因科技有限公司成立于2016年,由哥倫比亞大學博士后趙輝,歸國創(chuàng)辦的國家高新技術(shù)企業(yè)。擁有97項知識產(chǎn)權(quán)及實用技術(shù),業(yè)務遍布上海、重慶、深圳、北京等城市,總部在鄭州航空港區(qū)。
青光眼是一種以病理性高眼壓、視神經(jīng)萎縮、視野缺損和視力下降為特征的常見眼病。它是全球首位不可逆致盲眼病,主要病理表現(xiàn)為視網(wǎng)膜神經(jīng)節(jié)細胞的損傷和凋亡。據(jù)世界衛(wèi)生組織統(tǒng)計,到2040年,全球青光眼患者將增至1.118億。
外泌體:細胞間通信的“信使”
外泌體是一類由活細胞分泌的具有磷脂雙分子層結(jié)構(gòu)的囊泡,其內(nèi)攜帶RNA、DNA、蛋白質(zhì)、脂質(zhì)等多種信號分子,起到細胞間信號傳遞的作用。特別是來源于干細胞的外泌體,不僅包含豐富的生物活性物質(zhì),還具備促進組織修復、減少炎癥反應、抑制纖維化等獨特的功能。
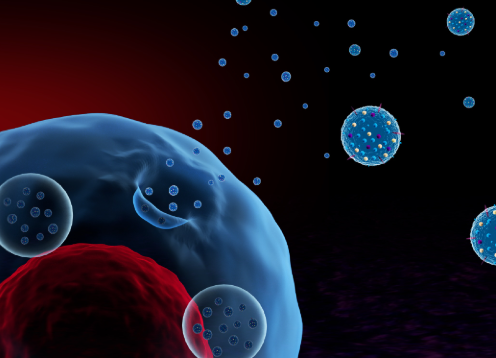
外泌體干預眼科疾病的機制
外泌體在眼科疾病治療中具有多重機制:
促進組織修復與再生:外泌體能夠攜帶促生長因子,促進角膜和視網(wǎng)膜等組織的修復。
抗炎作用:外泌體通過調(diào)節(jié)免疫系統(tǒng),能夠減少炎癥反應,在干眼癥和角膜炎等疾病中表現(xiàn)出顯著的抗炎效果。
減少纖維化與疤痕形成:外泌體能夠抑制纖維化過程,減少疤痕形成,有助于組織修復。
精準靶向遞送:外泌體具備較高的靶向性,能夠精準地將治療分子送至病變部位。

外泌體干預青光眼的文獻研究
近年來,外泌體在青光眼治療中的研究取得了顯著進展。例如,Perkumas等通過對小梁網(wǎng)細胞的外泌體進行蛋白質(zhì)譜鑒定,發(fā)現(xiàn)外泌體中包含多種小梁網(wǎng)細胞的特異性蛋白,表明外泌體可能參與眼壓調(diào)控。Liu等研究發(fā)現(xiàn),原發(fā)性開角型青光眼患者的外泌體基因表達存在差異,異常的外泌體轉(zhuǎn)運途徑可能是其潛在發(fā)病機制。

在動物實驗中,研究人員將骨髓間充質(zhì)干細胞來源的外泌體移植到青光眼動物模型的玻璃體中,發(fā)現(xiàn)外泌體能夠?qū)⑾嚓PmRNA(如miR-100-5P、miR-106A-5P等)轉(zhuǎn)運到視網(wǎng)膜神經(jīng)節(jié)細胞內(nèi),促進細胞存活,防止功能衰退,并對軸突有一定的保護作用。另一項研究利用間充質(zhì)干細胞衍生的外泌體治療青光眼大鼠模型,結(jié)果表明,每周和每月在玻璃體內(nèi)注射間充質(zhì)干細胞衍生的外泌體后,能夠顯著促進視網(wǎng)膜神經(jīng)節(jié)細胞的神經(jīng)保護作用。

總結(jié)
盡管外泌體在青光眼治療中展現(xiàn)出巨大的潛力,但目前仍處于研究階段。未來需要更多的研究和臨床試驗來驗證其安全性和有效性。隨著技術(shù)的不斷進步,外泌體有望成為青光眼治療的新手段,為患者帶來新的希望。