鄭州源創(chuàng)基因科技有限公司成立于2016年,由哥倫比亞大學(xué)博士后趙輝,歸國(guó)創(chuàng)辦的國(guó)家高新技術(shù)企業(yè)。擁有97項(xiàng)知識(shí)產(chǎn)權(quán)及實(shí)用技術(shù),業(yè)務(wù)遍布上海、重慶、深圳、北京等城市,總部在鄭州航空港區(qū)。
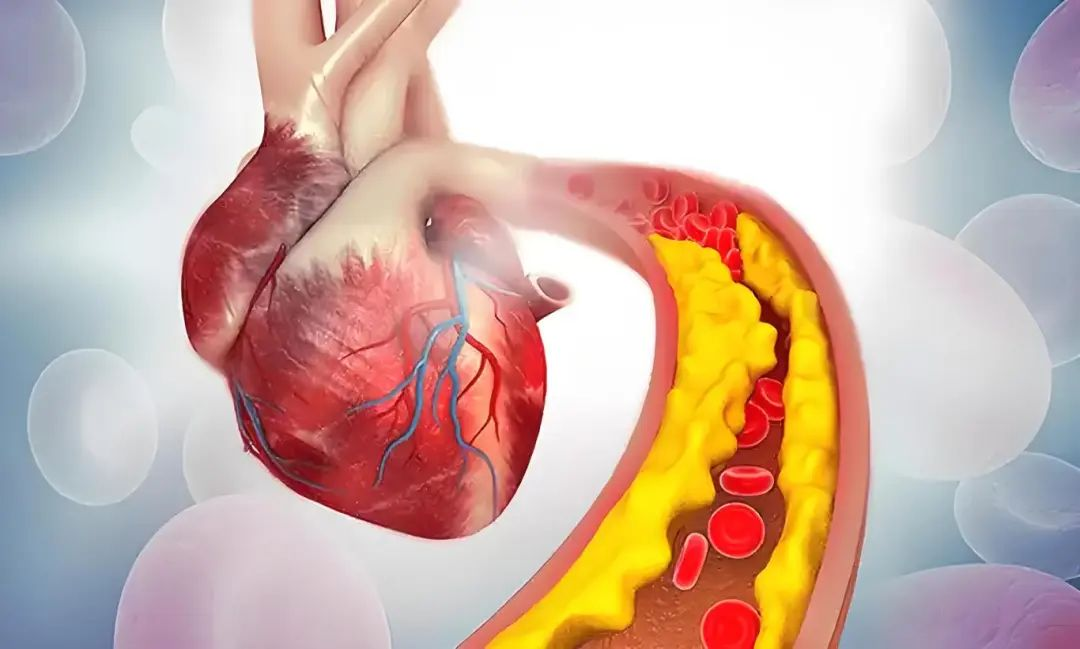
心血管疾病是全球健康的“頭號(hào)殺手”,在我國(guó)更是呈現(xiàn)爆發(fā)式增長(zhǎng)——患者數(shù)量高達(dá)3.3億,其中心力衰竭患者約890萬(wàn)。這些患者的五年死亡率超過(guò)50%,生存率甚至低于多種癌癥。
傳統(tǒng)藥物、介入治療和心臟搭橋手術(shù)雖能緩解癥狀,卻無(wú)法讓壞死的心肌細(xì)胞再生。當(dāng)疾病發(fā)展到終末期,心臟移植成為最后的選擇,卻又面臨著供體稀缺、創(chuàng)傷大和經(jīng)濟(jì)負(fù)擔(dān)重等難題。
干細(xì)胞療法的出現(xiàn),如同一道劃破黑暗的光芒,為心血管疾病患者帶來(lái)了前所未有的希望——通過(guò)再生醫(yī)學(xué)的力量,讓心肌細(xì)胞“死而復(fù)生”,重塑受損的心臟結(jié)構(gòu)。
干細(xì)胞修復(fù)心臟的奧秘
干細(xì)胞治療心血管疾病之所以備受矚目,關(guān)鍵在于其擁有三重修復(fù)機(jī)制。
分化再生能力是干細(xì)胞的核心“超能力”。當(dāng)干細(xì)胞被移植到心臟后,它們能夠分化成心肌細(xì)胞和血管內(nèi)皮細(xì)胞,直接替代受損的心肌組織,恢復(fù)心臟的收縮功能,同時(shí)重建受損的血管網(wǎng)絡(luò)。
旁分泌作用則是干細(xì)胞的“通訊系統(tǒng)”。它們分泌多種生長(zhǎng)因子和細(xì)胞因子,包括血管內(nèi)皮生長(zhǎng)因子(VEGF)、轉(zhuǎn)化生長(zhǎng)因子β(TGF-β)和成纖維細(xì)胞生長(zhǎng)因子(FGF),促進(jìn)血管新生和心肌細(xì)胞再生,改善心肌供血。
免疫調(diào)節(jié)功能展現(xiàn)了干細(xì)胞的“智慧”。通過(guò)釋放多種細(xì)胞因子,干細(xì)胞能減輕局部炎癥反應(yīng),改善組織愈合環(huán)境,防止進(jìn)一步的組織損傷,為心臟修復(fù)創(chuàng)造有利條件。
這些機(jī)制共同構(gòu)成了干細(xì)胞修復(fù)心臟的“三重奏”,不僅針對(duì)癥狀,更直擊疾病根源——受損的心肌組織本身。
全球突破心肌再生的重大進(jìn)展
2025年1月,德國(guó)哥廷根大學(xué)醫(yī)學(xué)中心和德國(guó)心血管研究中心在《Nature》雜志發(fā)表了一項(xiàng)里程碑式研究。他們使用誘導(dǎo)多能干細(xì)胞(iPSC)來(lái)源的心肌細(xì)胞和基質(zhì)細(xì)胞構(gòu)建了工程化心肌(EHM)同種異體移植物。

研究人員在心力衰竭的恒河猴體內(nèi)植入EHM后,觀察到其長(zhǎng)期留存達(dá)6個(gè)月,并顯著增強(qiáng)了心臟的收縮功能和射血分?jǐn)?shù),且未出現(xiàn)心律失常或腫瘤形成等副作用。
基于這一成功,研究團(tuán)隊(duì)進(jìn)行了首次人體臨床試驗(yàn)。結(jié)果令人振奮:一位晚期心力衰竭患者在接受EHM移植后,實(shí)現(xiàn)了真正的心肌再生,移植的心肌細(xì)胞在患者心臟中存活并發(fā)揮功能。
重塑“心”生,未來(lái)可期
干細(xì)胞治療心血管疾病的探索之路,正以前所未有的速度向前推進(jìn)。從實(shí)驗(yàn)室的精密設(shè)計(jì)到臨床研究的振奮成果,每一次突破都在印證著再生醫(yī)學(xué)改寫(xiě)“心病”治療格局的巨大潛力。盡管挑戰(zhàn)猶存,標(biāo)準(zhǔn)化、安全性?xún)?yōu)化和長(zhǎng)期療效驗(yàn)證仍是攀登路上的重要階梯,但科學(xué)界對(duì)此領(lǐng)域的信心與日俱增。
未來(lái)醫(yī)學(xué)將不再局限于藥物控制癥狀,而是直指病灶修復(fù)再生。當(dāng)干細(xì)胞療法廣泛應(yīng)用之日,我們或許將見(jiàn)證心血管疾病從“不治之癥”到“可逆之癥”的歷史性轉(zhuǎn)變。
參考資料:
[1]Barto lucci J, et al. (2017)*Safety and Efficacy of the Intravenous Infusion of Umbilical Cord Mesenchymal Stem Cells in Patients with Heart Failure: A Phase 1/2 Randomized Controlled Trial*
[2] Makkar RR, et al. (2012)*Intracoronary Cardiosphere-Derived Cells for Heart Regeneration after Myocardial Infarction (CADUCEUS): A Prospective, Randomised Phase 1 Trial*
[3]《中國(guó)心血管健康與疾病報(bào)告 2020》編寫(xiě)組 (2021)《中國(guó)心血管健康與疾病報(bào)告2020》要點(diǎn)解讀,期刊:中國(guó)心血管雜志
[4]天津醫(yī)科大學(xué)總醫(yī)院團(tuán)隊(duì) (2025)*CD73-expressing Endometrial Regenerative Cell-Derived Exosomes Mitigate Acute Cardiac Allograft Rejection through Regulating Adenosine Metabolism in Mice*
[5]https://mp.weixin.qq.com/s/ESQXW_uOFyNbFnfENHIWwg