鄭州源創(chuàng)基因科技有限公司成立于2016年,由哥倫比亞大學(xué)博士后趙輝,歸國創(chuàng)辦的國家高新技術(shù)企業(yè)。擁有97項(xiàng)知識(shí)產(chǎn)權(quán)及實(shí)用技術(shù),業(yè)務(wù)遍布上海、重慶、深圳、北京等城市,總部在鄭州航空港區(qū)。
近年來,越來越多的臨床研究證實(shí)了間充質(zhì)干細(xì)胞應(yīng)用于阿爾茲海默癥的安全性和有效性。
目前,全球阿爾茨海默病(AD)患者數(shù)已超過5500萬,盡管存在三款單抗藥物能夠一定程度上延緩病程,但均面臨“腦萎縮加速”的悖論:雖然能有效清除致病蛋白,卻不可避免地加速了腦萎縮。因此,治療抉擇在清除蛋白與保護(hù)腦結(jié)構(gòu)間搖擺不定,醫(yī)學(xué)界迫切需要一種雙贏的新療法。

2025年3月10日,《Nature Medicine》發(fā)布了突破性臨床研究,骨髓源間充質(zhì)細(xì)胞療法Laromestrocel在49例輕度阿爾茨海默病(AD)患者中取得了突破性進(jìn)展:不僅使海馬體的萎縮速度降低了61.9%,還實(shí)現(xiàn)了全腦體積48.4%的保護(hù)率,且整個(gè)過程中未出現(xiàn)任何淀粉樣蛋白相關(guān)影像異常(ARIA)的安全問題。

該試驗(yàn)于2021-2022年在美國10個(gè)醫(yī)學(xué)中心開展,招募49例輕度AD患者,按1:1:1:1比例分為4組,治療時(shí)長4個(gè)月,隨訪39周。其中,組1為安慰劑組,每月輸注一次安慰劑;組2首劑輸注2500萬細(xì)胞,后續(xù)3個(gè)月輸安慰劑;組3每月輸注2500萬細(xì)胞;組4每月輸注1億細(xì)胞。
在這項(xiàng)隨機(jī)雙盲試驗(yàn)中, Laromestrocel無論是單次還是多次輸注,治療組均展現(xiàn)出良好的安全性,沒有報(bào)告輸注相關(guān)反應(yīng)和超敏反應(yīng)。
更重要的是,laromestrocel顯著減緩了全腦和部分關(guān)鍵腦區(qū)的萎縮。與安慰劑組相比,所有治療組聯(lián)合分析時(shí),全腦體積的萎縮減緩了48.4%,另外,Laromestrocel不同劑量的治療組相對(duì)于安慰劑組的左側(cè)、右側(cè)和雙側(cè)海馬萎縮分別減少了62%、53%和59%,其中左側(cè)和雙側(cè)的減少達(dá)到了統(tǒng)計(jì)學(xué)顯著性。
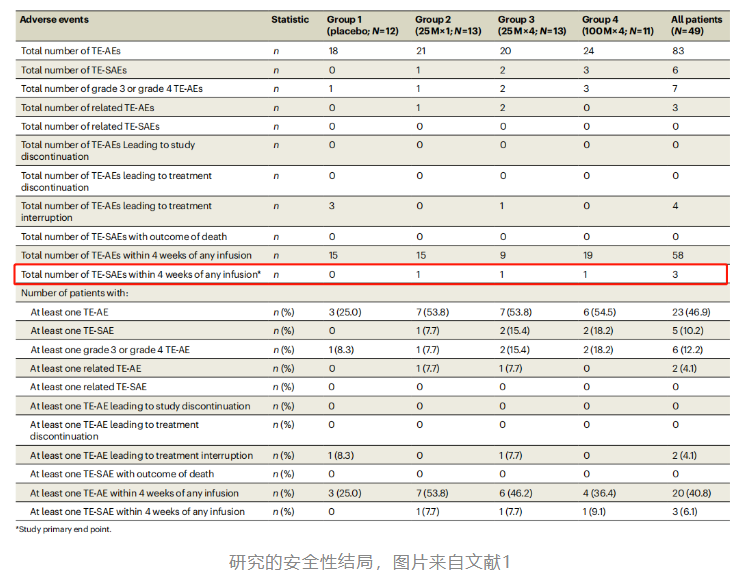
上述結(jié)果表明,對(duì)于輕度阿爾茨海默病患者,使用laromestrocel無論是單次還是多次給藥均是安全的,患者耐受性好,且laromestrocel有助于減緩患者腦萎縮速度、治療潛在認(rèn)知功能下降。研究人員推測更長的治療時(shí)間,將有助于延緩阿爾茨海默病的進(jìn)展。
Laromestrocel(通用名)是同種異體間充質(zhì)細(xì)胞(MSCs)療法,可以通過分泌生物活性因子,調(diào)節(jié)免疫反應(yīng)、抑制炎癥、促進(jìn)血管生成及組織修復(fù)。針對(duì)輕度AD患者,通過減緩腦萎縮和改善認(rèn)知功能發(fā)揮作用。臨床試驗(yàn)顯示可減少神經(jīng)炎癥、延緩海馬體萎縮。其AD適應(yīng)癥,被FDA認(rèn)定為再生醫(yī)學(xué)先進(jìn)療法(RMAT)和快速通道資格。
參考文獻(xiàn)
1.Rash, B.G., Ramdas, K.N., Agafonova, N. et al. Allogeneic mesenchymal stem cell therapy with laromestrocel in mild Alzheimer’s disease: a randomized controlled phase 2a trial. Nat Med (2025). https://doi.org/10.1038/s41591-025-03559-02.https://longeveron.com
【免責(zé)聲明】圖片及部分文字來源于網(wǎng)絡(luò),部分?jǐn)?shù)據(jù)本公眾號(hào)并未驗(yàn)證,旨在分享相關(guān)知識(shí),僅作信息交流之目的,平臺(tái)所轉(zhuǎn)載的所有的文章、圖片、音頻、視頻文件等資料的版權(quán)歸版權(quán)所有人所有,如涉及版權(quán)等問題,請(qǐng)聯(lián)系我們及時(shí)處理。文章內(nèi)容不作為相關(guān)醫(yī)療指導(dǎo)或用藥建議,僅供參考。