鄭州源創(chuàng)基因科技有限公司成立于2016年,由哥倫比亞大學(xué)博士后趙輝,歸國(guó)創(chuàng)辦的國(guó)家高新技術(shù)企業(yè)。擁有97項(xiàng)知識(shí)產(chǎn)權(quán)及實(shí)用技術(shù),業(yè)務(wù)遍布上海、重慶、深圳、北京等城市,總部在鄭州航空港區(qū)。
雄激素性脫發(fā) (androgenic alopecia,AGA)是一種常見的脫發(fā)類型,主要與遺傳和雄性激素水平有關(guān)。目前,市場(chǎng)上治療AGA的藥物存在副作用大、療效有限等問題。因此,尋找更加安全、有效的治療方案仍是該領(lǐng)域的重點(diǎn)研究方向。

研究發(fā)現(xiàn),雄激素性脫發(fā)(AGA)的發(fā)生與毛囊干細(xì)胞(HFSCs)微環(huán)境的失調(diào)或活性下降密切相關(guān),AGA患者的HFSCs并未完全喪失。在適宜的微環(huán)境條件下,重新激活HFSC有望恢復(fù)毛囊功能,實(shí)現(xiàn)毛發(fā)再生與脫發(fā)逆轉(zhuǎn)。
近年來,如何激活處于“沉睡”狀態(tài)的毛囊干細(xì)胞、重建毛囊微環(huán)境,成為脫發(fā)治療的新突破口。在這一方向上,干細(xì)胞及其分泌的外泌體因其再生潛能和免疫調(diào)節(jié)功能,引起了廣泛關(guān)注。
外泌體是細(xì)胞分泌的一種微小囊泡,富含生長(zhǎng)因子、信號(hào)蛋白和非編碼RNA等生物活性分子,能夠通過細(xì)胞間通信調(diào)節(jié)靶細(xì)胞的功能,在多種組織修復(fù)研究中表現(xiàn)出良好效果。
基于間充質(zhì)干細(xì)胞外泌體在組織修復(fù)領(lǐng)域的突出表現(xiàn),越來越多的研究團(tuán)隊(duì)開始探索其在促進(jìn)毛囊再生、干預(yù)脫發(fā)過程中的潛力。
2025年3月,同濟(jì)大學(xué)東方醫(yī)院轉(zhuǎn)化醫(yī)學(xué)研究中心的科研團(tuán)隊(duì)在《World Journal of Stem Cells》(《世界干細(xì)胞雜志》)上發(fā)表一篇題為“Mesenchymal stem cell exosomes enhance the development of hair follicle to ameliorate androgenetic alopecia”(間充質(zhì)干細(xì)胞外泌體促進(jìn)毛囊的發(fā)育,從而改善雄激素性脫發(fā))的文章,該研究評(píng)估了人類脂肪來源的間充質(zhì)干細(xì)胞外泌體 (hADSC-Exos) 和人類臍帶來源的間充質(zhì)干細(xì)胞外泌體 (hUCMSC-Exos) 在改善雄激素性脫發(fā)(AGA)中毛乳頭細(xì)胞增殖的潛力。
脂肪間充質(zhì)干細(xì)胞來源的外泌體中含有包括細(xì)胞周期調(diào)控因子CDC42在內(nèi)的232種關(guān)鍵蛋白,這些特征均表明其在改善毛囊周圍微環(huán)境方面具有獨(dú)特優(yōu)勢(shì)。
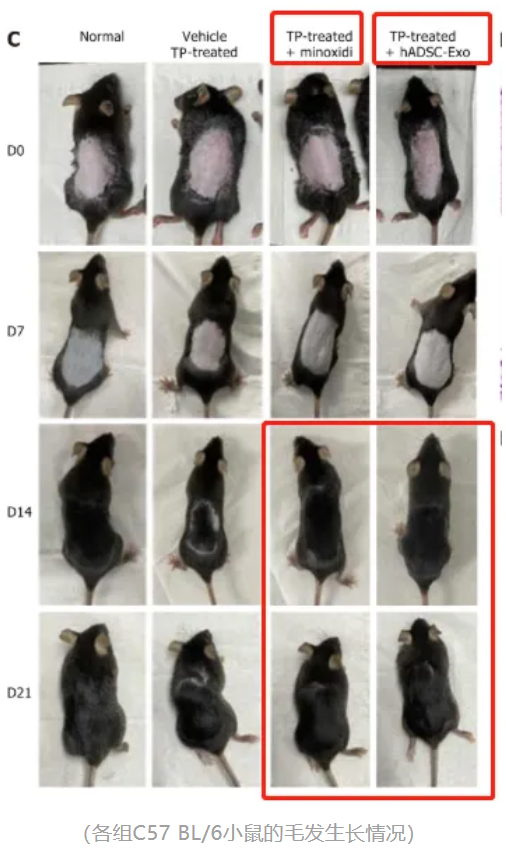
為了觀察皮膚中毛囊的初始形態(tài)發(fā)生,所有小鼠背部毛發(fā)均被剃掉。
研究團(tuán)隊(duì)通過持續(xù)21天的動(dòng)態(tài)觀察發(fā)現(xiàn),模型對(duì)照組(陰性對(duì)照組)小鼠皮膚持續(xù)呈現(xiàn)粉紅色(表明毛囊仍處于休止期),而外泌體治療組在14天時(shí)已顯現(xiàn)深灰色皮膚(毛囊進(jìn)入生長(zhǎng)期的特征),且毛發(fā)生長(zhǎng)覆蓋率與米諾地爾組基本持平。組織病理學(xué)檢測(cè)顯示,外泌體治療組毛囊數(shù)量顯著增加,處于生長(zhǎng)期的毛囊比例較模型組提高近3倍。
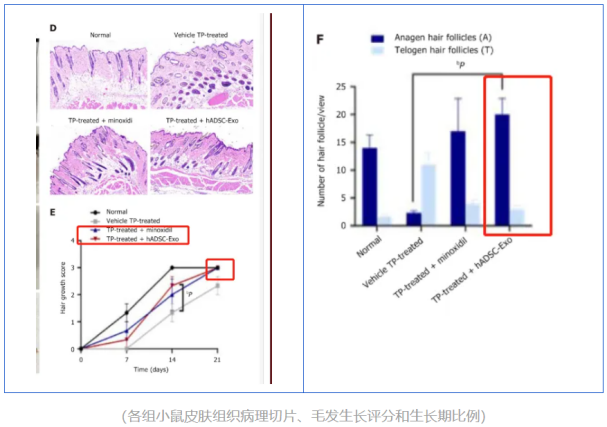
研究團(tuán)隊(duì)通過細(xì)胞實(shí)驗(yàn)驗(yàn)證,hADSC-Exos通過調(diào)控CDC42蛋白激活經(jīng)典Wnt/β-catenin信號(hào)通路,抑制糖原合酶激酶-3β活性,從而促進(jìn)毛乳頭細(xì)胞的增殖與遷移,逆轉(zhuǎn)雄激素誘導(dǎo)的毛囊休眠。
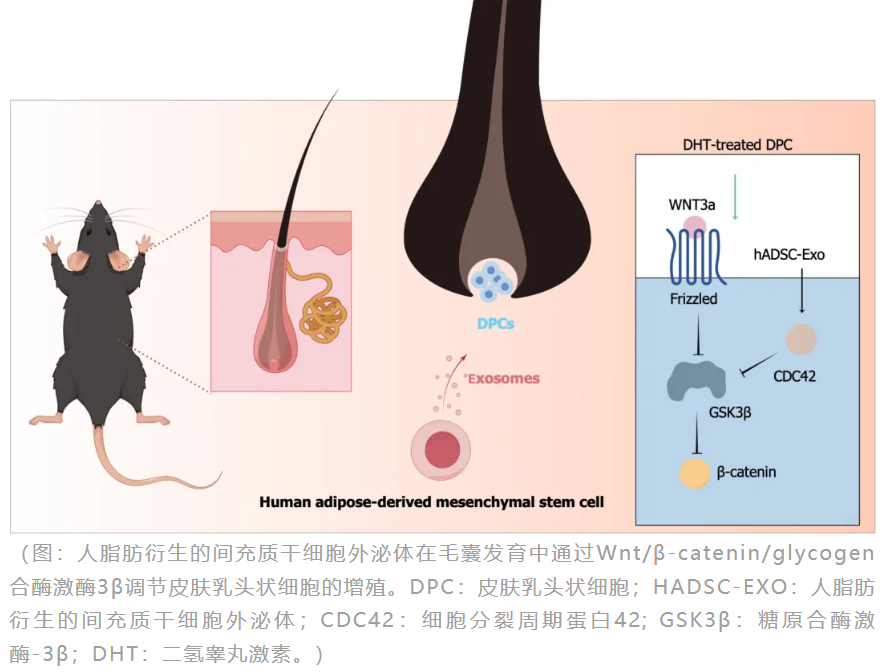
該研究表明,hADSC-Exos通過調(diào)控毛乳頭細(xì)胞功能促進(jìn)毛囊再生,在雄激素性脫發(fā)治療中展現(xiàn)出顯著潛力。該發(fā)現(xiàn)為開發(fā)新型無創(chuàng)性脫發(fā)治療方案提供了重要理論依據(jù),相較于傳統(tǒng)藥物療法,干細(xì)胞外泌體具有更好的生物相容性和靶向調(diào)節(jié)優(yōu)勢(shì)。
外泌體作為細(xì)胞間通訊的關(guān)鍵介質(zhì),可攜帶核酸、蛋白質(zhì)等多種生物活性分子,靶向調(diào)控與激活毛囊干細(xì)胞功能,促進(jìn)其增殖與分化,同時(shí)促進(jìn)受損毛囊的結(jié)構(gòu)修復(fù)并延長(zhǎng)毛發(fā)生長(zhǎng)期。此外,外泌體的抗炎特性能夠重塑頭皮微環(huán)境,有效抑制二氫睪酮(DHT)介導(dǎo)的毛囊萎縮信號(hào)通路,從多維度為毛囊提供保護(hù)性調(diào)控。
這項(xiàng)關(guān)于脂肪干細(xì)胞外泌體治療雄激素性脫發(fā)的研究,不僅為醫(yī)學(xué)界提供了新的治療思路和方法,也為廣大脫發(fā)患者帶來了新的希望。隨著研究的深入和技術(shù)的不斷進(jìn)步,相信脂肪間充質(zhì)干細(xì)胞來源的外泌體在脫發(fā)治療領(lǐng)域的應(yīng)用前景將越來越廣闊。
參考文獻(xiàn)
[1]Mesenchymal stem cell exosomes enhance the development of hair follicle to ameliorate androgenetic alopecia
Fu Y, Han YT, Xie JL, Liu RQ, Zhao B, Zhang XL, Zhang J, Zhang J. Mesenchymal stem cell exosomes enhance the development of hair follicle to ameliorate androgenetic alopecia. World J Stem Cells 2025; 17(3): 102088 [PMID: 40160691 DOI: 10.4252/wjsc.v17.i3.102088]
[2]https://mp.weixin.qq.com/s/5FiIjnx2PCIbG378Me6OJw